CRISPR/Cas heißt das Zauberwort in den Laboren weltweit, oder kurz: Genschere. Einfach und präzise in der Anwendung, preisgünstig in der Herstellung. Die neuartige Methode ist ein Verfahren des Genome Editing, dem gezielten Umschreiben von Erbinformationen, und könnte die Gentechnik revolutionieren. CRISPR/Cas – wie geht das, was kann es und wo sind seine Grenzen?
Aufbau und Funktionsweise von CRISPR/Cas
Viele Bakterien besitzen in ihrer DNA besondere Teilbereiche, sogenannte clustered regularly interspaced palindromic repeats, kurz CRISPR. Hier wechseln sich repetierende und variable Sequenzmotive (repeats und spacer) ab. Die benachbarten Gene heißen CRISPR-assoziierte Gene, abgekürzt cas. Diese stellen unterschiedliche Proteine her, die für das Funktionieren des Wirkkomplexes CRISPR/Cas notwendig sind. Wird das Bakterium von einem Krankheitserreger infiziert, werden Stücke der schädlichen Fremd-DNA in die CRISPR-Region aufgenommen (spacer). Sie dienen bei einer erneuten Infektion als Erkennungssignal und leiten die Zerstörung des Angreifers ein, vergleichbar mit einem Immunsystem. Das Enzym Cas9 übernimmt hierbei die Aufgabe einer Genschere. Es durchtrennt die Fremd-DNA und macht sie unschädlich.
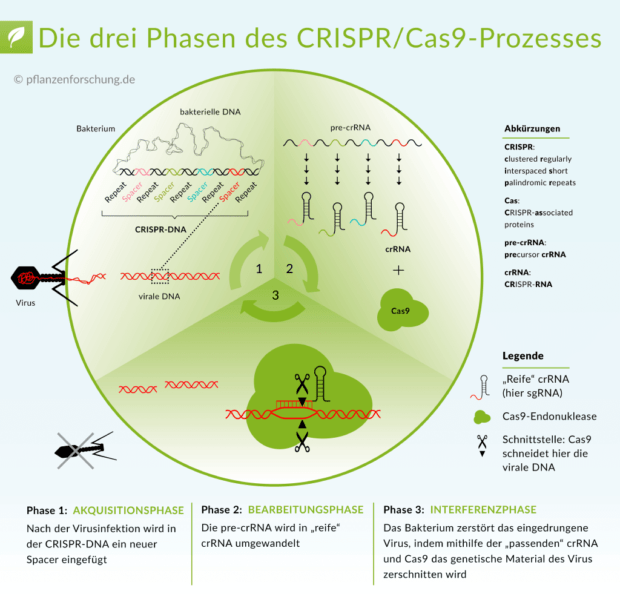
Die genetische Information der CRISPR-Region wird als kurze Nukleotidsequenz (crRNA) abgelesen. In Verbindung mit dem Cas-Protein dient sie als guide-RNA (gRNA), die das Enzym zu seinem Einsatzort führt. Ähnlich einem Klettverschluss bindet die gRNA an passende Zielsequenzen des Angreifers und das gebundene Enzym Cas9 zerschneidet die Fremd-DNA.
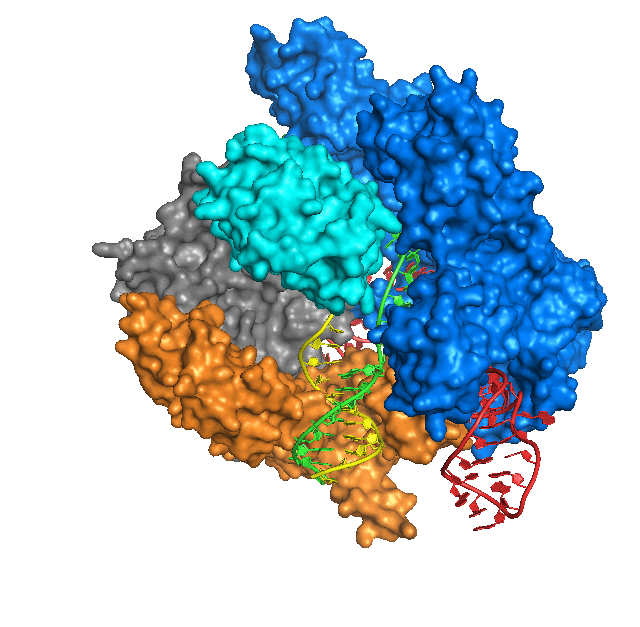
Anwendung des CRISPR/Cas-Systems
Die Fähigkeit, DNA an einer definierten Position zu schneiden, macht CRISPR/Cas für die Wissenschaft interessant und auch für das Gentechnikgesetz. Beliebige Nukleotidsequenzen können als gRNA eingefügt und prinzipiell in jedem Organismus angewendet werden. Voraussetzung ist, dass die Sequenz der Ziel-DNA bekannt ist. Ein Konstrukt aus gRNA und Cas-Protein wird in einen Zellkern eingebracht und die Genschere durchtrennt dort die DNA an gewünschter Stelle.
Diese Schnittstelle ist nun der Arbeitsplatz der Wissenschaftler. Hier können Gene eingefügt, ausgeschaltet oder reguliert werden. Durch zelleigene Reparaturmechanismen versucht die Zelle, den Bruch zu schließen. Bekommt sie eine Vorlage für die DNA-Reparatur angeboten, so fügen Enzyme ein neues Gen in die Schnittstelle ein (homologe Rekombination). In Abwesenheit einer Vorlage werden die zerbrochenen Stränge fehlerhaft zusammengefügt und das betroffene Gen verliert seine Funktion (nicht-homologe Rekombination).
CRISPR/Cas im Unterschied zu anderen Techniken
DNA-Modifikationen wurden bislang durch mikrobielle Vektorsysteme (vgl. Klonierung, Transgene Pflanzen) oder durch Mutagenese (Behandlung mit Chemikalien, Strahlung) erreicht. Grundlegendes Problem der klassischen Methoden ist, dass nicht vorhersagbar ist, an welcher Stelle im Genom die Veränderungen stattfinden. Sie könnten unbeabsichtigt intakte Gene zerstören oder krankhaftes Zellwachstum auslösen. Langwierige Studien sind notwendig, um geeignete Individuen zu identifizieren und ihre Unbedenklichkeit zu dokumentieren. Bei tierischen Organismen sind viele Experimente aufgrund technischer Probleme und ethischer Bedenken nicht durchführbar.
Größere Präzision verspricht das Genome Editing mit Hilfe künstlicher zusammengesetzter Enzym-Komplexe, sogenannter Nukleasen, zu denen auch CRISPR/Cas-Systeme gehören. Zinkfinger-Nukleasen (ZNF) oder TAL-Effektor-Nukleasen (TALENs) sind etablierte Werkzeuge und befinden sich in der klinischen Prüfung für verschiedene medizinische Anwendungen. Ihre Effektivität ist mäßig, die Herstellung teuer, die Nutzung bleibt auf größere Institute beschränkt.
CRISPR/Cas bietet Chancen und birgt Risiken
Punktgenau jedes beliebige Gen verändern und das restliche Genom nicht beeinträchtigen. Minimalinvasive Biotechnologie, die von natürlichen Mutationsvorgängen kaum unterscheidbar ist und rechtlich nicht als Gentechnik eingestuft wird. Das ist der Traum von CRISPR/Cas.
Seit ihrer Veröffentlichung hat die Methode alle Wissenschaftszweige erfasst. Zu verlockend ist diese einfache und preiswerte Technik, zu rasant das Rennen um wissenschaftliche Profilierung. Die Gesetzgebung hinkt der neuen Gentechnik hinterher. Schnell waren rote Linien überschritten und Eingriffe an menschlichen Keimbahnen vorgenommen worden. Hierzulande sind derartige Versuche verboten, andere Länder sehen das nicht so eng. Umso wichtiger ist die Debatte darüber, was erlaubt ist und was verboten bleiben muss. Wissenschaftler selbst warnen vor übertriebenen Erwartungen und überstürzten Experimenten.
Aktuelle Projekte befassen sich mit der Erzeugung von Krankheitsresistenzen für Nutzpflanzen und -tiere. Erste Studien offenbaren auch Schwachstellen, wie beispielsweise off-target-Ereignisse, bei denen zusätzliche, ungeplante DNA-Schnitte erfolgen. Das System muss sich nun in der Praxis beweisen, optimiert und den unterschiedlichen Nutzungsfeldern angepasst werden. Wenn das gelingt, bietet CRISPR/Cas großes Potential für Anwendungen in Pflanzenzüchtung, Gentherapie und Forschung.